ACIDI GRASSI E PREVENZIONE DEL DIABETE

![]()
Sindrome metabolica
Le malattie croniche non trasmissibili come malattie cardiache, cancro e diabete rappresentano le principali cause di mortalità nel mondo. Il comune denominatore sembra essere lo stile di dieta “occidentale” (Western diet), fatta di cibo con ingredienti di scarsa qualità e provenienti da processi chimici o non sostenibili, che ha fatto aumentare drasticamente l’incidenza delle disfunzioni metaboliche [1].
Sebbene siamo portati a pensare che sovrappeso e obesità portino a malattie croniche, in realtà molte persone normopeso già presentano sintomi collegabili alla sindrome metabolica: dislipidemia, ipertensione, iperglicemia, insulino-resistenza, steatosi epatica non alcolica.
L’insulino-resistenza
È ormai ampiamente dimostrato da studi epidemiologici che l’eccessivo consumo di zucchero può essere una condizione comune per i sintomi della sindrome metabolica, come ipertensione, ipertrigliceridemia, steatosi epatica, insulino-resistenza.
Eccessivi e prolungati livelli di glucosio nel sangue portano a una riduzione della sensibilità tissutale all’insulina, causando una ipersecrezione di quest’ultima da parte del pancreas nel tentativo di mantenere l’omeostasi del glucosio (iperinsulinemia compensativa). Questa condizione alla fine si traduce nell’ “esaurimento” delle cellule beta del pancreas, con riduzione della secrezione di insulina e, infine, sviluppo del diabete.
Le anomalie metaboliche più rilevanti si osservano nei tessuti sensibili allo stimolo dell’insulina: tessuto adiposo, fegato e muscoli.
- in condizioni normali, il tessuto adiposo è responsabile dell’accumulo di gocce di lipidi intracellulari, dai quali ottenere energia per mobilizzazione a seguito di stimolazione data dall’insulina. Ma quando la cellula adipocitaria oltrepassa il limite fisiologico di accumulo di grasso intracellulare, il suo destino è quello di sdoppiarsi diventando disfunzionale, smettendo di produrre adipochine insulino-sensibilizzanti (come l’adiponectina) e promuovendo ulteriormente la resistenza all’insulina degli altri tessuti, oppure andare incontro a morte programmata richiamando una risposta immunitaria.
- in condizioni normali, il muscolo è responsabile della captazione dell’80% del glucosio postprandiale. Invece in caso di insulino-resistenza periferica (muscolare), l’omeostasi plasmatica del glucosio peggiora fortemente. La situazione viene ulteriormente aggravata dall’aumentata disponibilità di acidi grassi rilasciati in circolo dal tessuto adiposo disfunzionale. Mentre inizialmente il muscolo può usare questi acidi grassi per scopi energetici, a lungo andare le cellule perdono questa flessibilità metabolica, la beta-ossidazione degli acidi grassi diventa inefficiente e si formano specie lipotossiche che peggiorano ulteriormente il metabolismo muscolare.
- in condizioni normali, circa il 60% degli acidi grassi che arrivano al fegato derivano dal tessuto adiposo. In caso di disfunzione adipocitaria, si ha un eccessivo afflusso di acidi grassi che vengono accumulati sotto forma di trigliceridi creando un deposito eccessivo noto come steatosi. Possono verificarsi i fenomeni di parziale ossidazione dei trigliceridi e di aumentata formazione delle aggregazioni lipidiche piàù ricche in triglicerdidi, come LDL e VLDL responsabili di ipertrigliceridemia con esiti non favorevoli.
Tutto considerato, l’insorgere di insulino-resistenza nei tessuti bersaglio sensibili all’insulina provoca importanti anomalie metaboliche, come iperglicemia e ipertrigliceridemia, caratteristiche comuni della sindrome metabolica.
Insulino-resistenza e membrana cellulare
Molte evidenze sperimentali suggeriscono una stretta associazione tra la sensibilità all’insulina e composizione lipidica della membrana cellulare.
Dal momento che la segnalazione dell’insulina avviene per interazione dell’insulina con il suo recettore posizionato nella membrana cellulare, la composizione degli acidi grassi di membrana e le proprietà chimico-fisiche che essi determinano sono responsabili della modulazione della funzione recettoriale nella via di segnalazione dell’insulina.
Due sono i principali aspetti che mettono in relazione la composizione di membrana con l’insulino-resistenza:
1) NUMERO E AFFINITÀ DEI RECETTORI PER L’INSULINA
È stato dimostrato che la diminuzione della fluidità della membrana dovuta all’aumento del contenuto di acidi grassi saturi (SFA) nei fosfolipidi ostacola l’assemblaggio dell’apparato proteico di segnalazione dell’insulina sulla superficie cellulare per limitata mobilità delle proteine nel doppio strato lipidico.
2) CAPTAZIONE DEL GLUCOSIO PLASMATICO
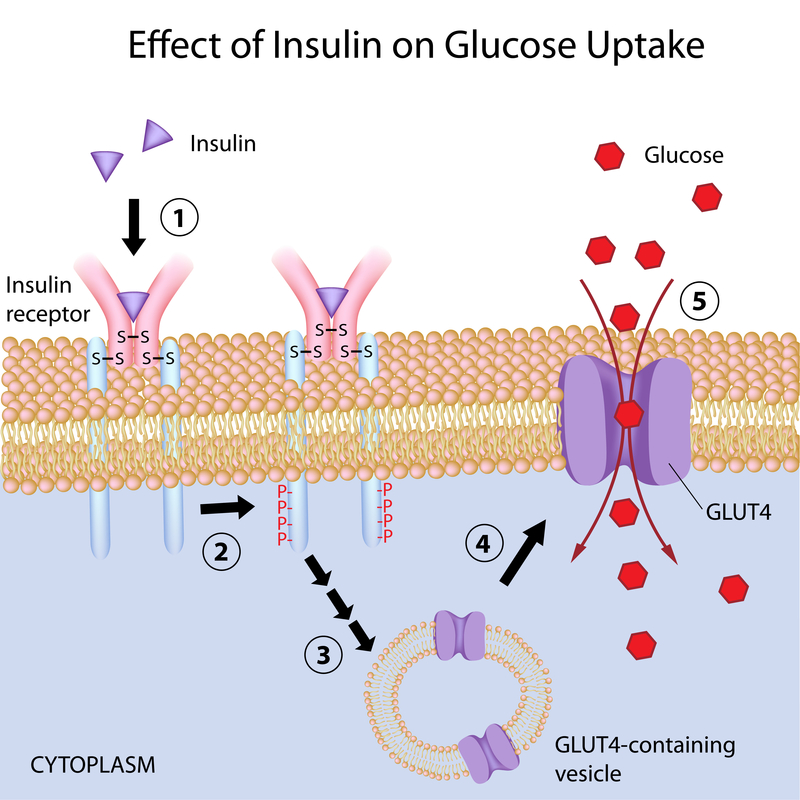
Il glucosio entra nelle cellule grazie a proteine trasportatrici specifiche chiamate GLUT (trasportatori del glucosio). Il GLUT4, presente negli adipociti e nelle cellule muscolari, differisce dagli altri trasportatori della stessa famiglia, in quanto circa il 90% è sequestrato in vescicole intracellulari che si mobilizzano solo quando l’insulina lega il recettore sulla membrana plasmatica. A quel punto, le vescicole contenti GLUT4 migrano verso la membrana con cui si fondono. Una volta localizzati sulla membrana plasmatica, i trasportatori GLUT4 facilitano successivamente l’entrata del glucosio plasmatico nella cellula.
Questo meccanismo di trasporto attraverso le membrane può essere fortemente influenzato dalla fluidità della membrana. Infatti, è stato dimostrato che una diminuzione della fluidità di membrana ostacola la fusione delle vescicole con la membrana plasmatica e l’esposizione del GLUT4 sulla superficie cellulare, pregiudicando così la sensibilità all’insulina di cellule muscolari ed adipocitarie.
Grassi alimentari e insulino-resistenza
Studi su modelli animali e sull’uomo hanno accumulato un numero impressionante di prove che stabiliscono la connessione tra grassi alimentari, profili lipidici di membrana e resistenza all’insulina (Membrane theory of Diabetes [2]). La qualità e la quantità dei grassi assunti con la dieta può, infatti, favorire o contrastare l’insorgere dell’insulino-resistenza attraverso l‘incorporazione nelle membrane cellulari e il mantenimento della struttura di membrana.

Un equilibrato apporto di grassi con la dieta si può rivelare cruciale nel ripristino e nel mantenimento della sensibilità all’insulina, soprattutto se si considera che le disfunzioni metaboliche nei tessuti target (come abbiamo visto: tessuto adiposo, muscolo e fegato) iniziano a verificarsi decenni prima della diagnosi di diabete di tipo 2.
– il consumo di acidi grassi saturi SFA e trans con la dieta modifica la composizione della membrana cellulare determinando un aumento della rigidità del doppio strato lipidico. Questo può ostacolare l’esposizione del GLUT4 e la funzione del recettore per l’insulina nei tessuti bersaglio. Inoltre, gli SFA tendono ad accumularsi in depositi intracellulari di difficile mobilizzazione. Quando usati come fonte energetica, sono parzialmente ossidati nei mitocondri, favorendo così la formazione di specie reattive dell’ossigeno, di prodotti lipotossici e la compromissione della funzione delle cellule muscolari ed epatiche. Lo stesso vale per le diete ricche di carboidrati dal momento che il glucosio è rapidamente convertito in SFA (acido palmitico, 16:0) attraverso la de novo lipogenensi nel fegato e negli adipociti.
– la sostituzione dei grassi saturi con acidi grassi monoinsaturi (MUFA) nella dieta migliora l’insulino-sensibilità sia nei soggetti sani che nei soggetti diabetici. L’olio extravergine di oliva, in quanto principale fonte di MUFA (acido oleico) nella nostra alimentazione, determina un migliore controllo glicemico e migliora l’insulino-sensibilità rispetto a chi fa principalmente uso di olio di semi di girasole (ricco di PUFA omega-6). Inoltre, gli acidi grassi MUFA sono più efficientemente ossidati nei mitocondri per produrre energia e, al tempo stesso, favoriscono la completa ossidazione degli acidi SFA, prevenendo così la formazione di radicali liberi nella cellula.
– diete con un basso rapporto omega-6/omega-3 si sono dimostrate efficaci nel contrastare l’insulino-resistenza adipocitaria e muscolare. Questo è dovuto sia all’aumento di fluidità di membrana per incorporazione di acidi grassi polinsaturi (PUFA) omega-3 ad alto grado di insaturazione. Inoltre, l’effetto insulino-sensibilizzante si ha anche grazie allo stimolo dell’espressione dei geni GLUT4 e del recettore dell’insulina attraverso l’azione su specifici fattori di trascrizione.
Articolo a cura del Gruppo Redazionale di Lipinutragen
I consigli alimentari presenti nell’articolo non sono da intendersi sostitutivi di un piano alimentare personalizzato e sono da adattare ai casi specifici.
Bibliografia
[1] “Health effects of dietary risks in 195 countries, 1990–2017: a systematic analysis for the Global Burden of Disease Study 2017” DOI: https://doi.org/10.1016/S0140-6736(19)30041-8
[2] Pilon M. “Revisiting the membrane-centric view of diabetes” Lipids in Health and Disease (2016) 15:167.
Per approfondire
Foto: 123RF Archivio Fotografico: 126263301 : ©artinspiring | 70028082 : @moremar
- Il 9 Novembre 2022